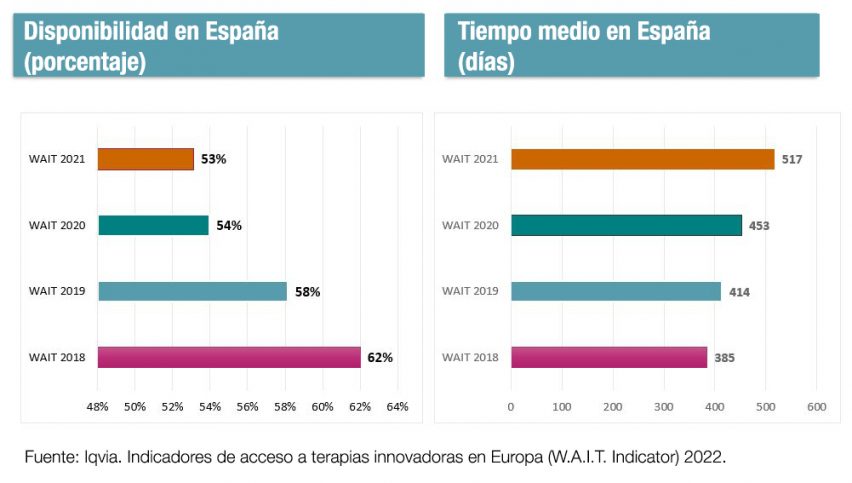
Según el informe anual ‘Indicadores de acceso a terapias innovadoras en Europa (W.A.I.T. Indicator)’, encargado por la Federación Europea de Asociaciones de la Industria Farmacéutica (EFPIA), a finales de 2021, el tiempo medio que transcurría desde que un nuevo medicamento era aprobado por las autoridades europeas hasta que estaba disponible para su uso en España era de 517 días, o lo que es lo mismo, más de 17 meses. Además, esa demora creció con respecto a 2020, cuando era de 453 días.
Los tiempos de aprobación en España siguen siendo más largos que en países como Alemania, donde la espera es de 133 días; Francia, 240 días; Inglaterra, 340, o Italia, 429 días. Pese a todo, nuestro país se sitúa por encima de la media de los 39 países analizados en el informe, 27 de los cuales pertenecen a la Unión Europea.
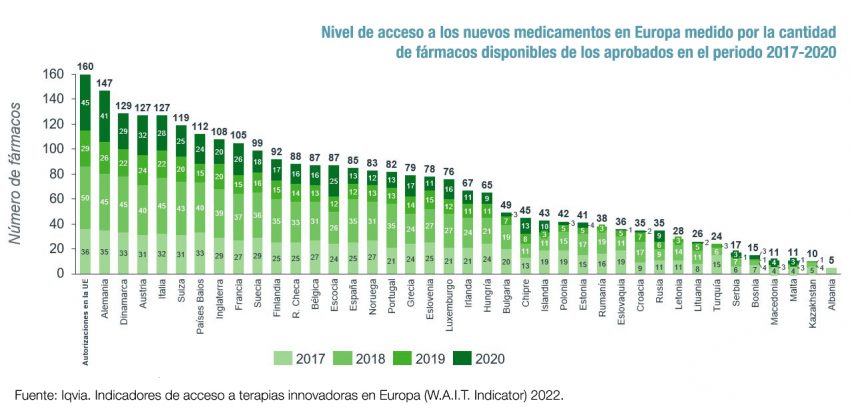
El otro indicador que mide el estudio es la disponibilidad, es decir, el número de nuevos medicamentos que son incluidos en la financiación pública y puestos a disposición de los pacientes. Ese porcentaje es también el más bajo de los grandes países europeos. Así, a 1 de enero de 2022 estaban disponibles en España 85 de los 160 medicamentos aprobados en la UE en el periodo 2017-2020, es decir, el 53%. Mientras, en Alemania este porcentaje era del 92%; en Italia, del 79%; en Inglaterra, del 68%, y en Francia, del 66%. Desde el año 2018, el porcentaje de disponibilidad en España ha disminuido nueve puntos porcentuales.
Además, los datos revelan que España tiene también el mayor porcentaje de disponibilidad restringida, con un 41%. Es decir, 4 de cada 10 medicamentos disponibles en nuestro país lo están con algún tipo de restricción en su uso. Este porcentaje es del 1% en Alemania, del 13% en Italia, del 15% en Francia y del 39% en Inglaterra.
En España, según el citado informe, el tiempo medio en 2021 para acceder a los nuevos medicamentos oncológicos ha aumentado en 74 días respecto a 2018, y la demora ya alcanza los 469 días. Además, el porcentaje de disponibilidad de los tratamientos oncológicos aprobados en Europa entre 2017 y 2020 es en nuestro país del 61% (están disponibles 25 de los 41 medicamentos autorizados en este periodo), el porcentaje más bajo de nuestro entorno (en Alemania es del 100%; en Italia, del 90%; en Inglaterra, del 85%, y en Francia, del 80%).
En el caso de los medicamentos huérfanos, la demora media en 2021 para el acceso en España ha aumentado en 184 días respecto al informe de 2018 y se sitúa en los 696 días, casi dos años de retraso. Además, sólo el 44% (25 de 57) de estos tratamientos autorizados en Europa en los últimos cuatro años están disponibles en nuestro país. También es el porcentaje más bajo de los países de referencia: Alemania tiene el 95%; Italia, el 75%; Francia, el 72%, e Inglaterra, el 61%.
Humberto Arnés, director general de la Asociación Nacional Empresarial de la Industria Farmacéutica en España (Farmaindustria), considera que, “como muestran estos datos, tenemos un problema estructural en el procedimiento de evaluación y financiación, que no es tan ágil como el de los países con los que debemos compararnos”.
Para Arnés, “España debe aspirar a estar entre los países que mejor acceso proporcionan a los nuevos tratamientos. Es responsabilidad de todos ponerlos a disposición de los profesionales sanitarios en el plazo más corto posible para que puedan beneficiarse los pacientes. Por eso abogamos por trabajar junto con el Ministerio de Sanidad para conseguir este objetivo común y superar con un procedimiento más eficiente los cuellos de botella existentes en el procedimiento de aprobación de medicamentos”.