El cáncer de vejiga tiene una de las tasas de incidencia más elevadas del mundo. A pesar de no tener una elevada mortalidad, casi la mitad de estos tumores vuelven a aparecer al cabo de 5 años. De hecho, su tasa de recurrencia asciende al 70%. Desde hace más de 30 años, con la finalidad de evitar las recurrencias se emplea un tipo de inmunoterapia de la que se beneficia cerca del 50 % de los pacientes; sin embargo, no existe todavía un indicador para predecir quiénes responderán adecuadamente a este tratamiento.
Ahora, un estudio publicado en la prestigiosa revista Nature Nanotechnology muestra cómo un equipo de investigación ha sido capaz de reducir en un 90% el tamaño de tumores de vejiga en ratones administrando una sola dosis de nanorrobots propulsados por urea. Estas diminutas nanomáquinas están formadas por una esfera porosa de sílica. En su superficie, incorporan diversos componentes con funciones específicas. Uno de ellos es la enzima ureasa, una proteína que reacciona con la urea, presente en la orina, haciendo que la nanopartícula sea capaz de propulsarse. Otro componente clave es el yodo radioactivo, un radioisótopo utilizado comúnmente para el tratamiento localizado de tumores.
El trabajo, liderado por el Instituto de Bioingeniería de Cataluña (IBEC) y el CIC biomaGUNE y desarrollado con la colaboración del Instituto de Investigación Biomédica (IRB Barcelona) y de la Universitat Autònoma de Barcelona (UAB), abre la puerta a nuevos tratamientos para el cáncer de vejiga que reduzcan el tiempo de hospitalización, lo que implicaría un menor coste y una mayor comodidad para el paciente. Y es que, lo habitual en pacientes con este tipo de tumores es que vayan entre 6 y 14 veces al hospital.
El siguiente paso, en el que ya está trabajando el equipo, es estudiar si estos tumores vuelven a aparecer tras el tratamiento.
Un viaje al interior de la vejiga
En investigaciones previas, los científicos confirmaron que la capacidad de autopropulsión de los nanorrobots les permitía alcanzar todas las paredes de la vejiga. Esta característica supone una ventaja respecto al procedimiento actual, donde una vez administrado el tratamiento directamente en la vejiga, el paciente debe cambiar de posición cada media hora para conseguir que el fármaco llegue a todas las paredes.
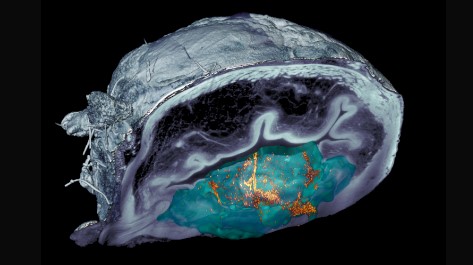
El nuevo trabajo va más allá al demostrar no solo la movilidad de las nanopartículas en la vejiga, sino también su acumulación específica en el tumor. Esto fue posible gracias a diferentes técnicas, incluyendo imágenes médicas de tomografía por emisión de positrones (PET) de los ratones, así como imágenes de microscopía sobre los tejidos extirpados tras la finalización del estudio. Estas últimas se tomaron mediante un sistema de microscopía de fluorescencia desarrollado específicamente para este proyecto en el IRB Barcelona. El sistema permite observar la vejiga completa, escaneando las distintas capas del órgano para luego obtener una reconstrucción en 3D.
“El innovador sistema óptico que hemos desarrollado, nos permitió, anular la luz que reflejaba el propio tumor y así identificar y localizar las nanopartículas en todo el órgano, sin un marcaje previo, a una resolución sin precedentes. Así vimos que los nanorrobots no solo alcanzaban el tumor, sino que lograban acceder a su interior, para favorecer así la actuación del radiofármaco”, explica Julien Colombelli, líder de la plataforma científica de Microscopía Digital Avanzada del IRB Barcelona.
Descifrar por qué los nanorrobots son capaces de acceder al interior del tumor fue un desafío. Los nanorrobots no contienen anticuerpos específicos para reconocer el tumor, y normalmente, el tejido tumoral es más rígido que el tejido sano. «Sin embargo, observamos que estos nanorrobots tienen la capacidad de descomponer la matriz extracelular del tumor al aumentar localmente el pH mediante una reacción química de autopropulsión. Este fenómeno podría favorecer una mayor penetración tumoral y resultó ser beneficioso para lograr una acumulación preferencial en el tumor”, detalla Meritxell Serra Casablancas, co-primera autora del estudio e investigadora del IBEC.
Así, los científicos llegaron a la conclusión de que los nanorrobots chocan con el urotelio como si fuera una pared, pero en el tumor, al ser más esponjoso, penetran y se acumulan en su interior. Un factor clave es la movilidad de los nanobots, que aumenta la probabilidad de que lleguen al tumor.